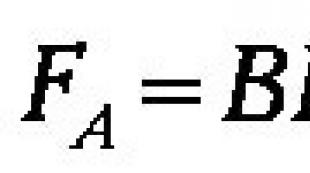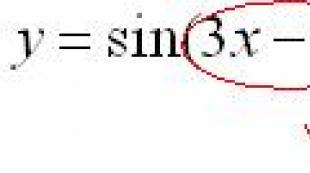Инфекционная доза. Инфицирующая доза
Вероятность развития инфекционного заболевания в значительной степени определяют:
Ø Видовые свойства возбудителя .
Ø Количество возбудителя – при попадании в организм незначительного числа патогенных микроорганизмов их обычно эффективно элиминируют защитные силы организма, для развития заболевания необходима инфицирующая доза возбудителя.
Инфицирующая доза возбудителя (Di ) – это минимальное количество микробных клеток, способных вызвать инфекционный процесс.
Ø Не менее значимы пути и место проникновения возбудителя в организм .
Входные ворота инфекции – ткани, лишенные физиологической защиты против конкретного вида микроорганизма, служат местом его проникновения в макроорганизм.
Например, слизистая оболочка трахеи и бронхов являются входными воротами пневмококков, вирусов гриппа, кори и др; слизистая оболочка кишечного тракта – для шигелл, сальмонелл, холерного вибриона; цилиндрический эпителий мочеполового тракта – для гонококков, уретральных микоплазм, хламидий. Ряд возбудителей проникает в организм несколькими путями (стафилококки, протеи, чума и др.) – для них характерен пантропизм .
Ø На развитие инфекционного процесса и его тяжесть существенно влияет и скорость размножения возбудителя .
Роль макроорганизма в развитии инфекционного процесса
Возникновение инфекционного заболевания и особенности его клинического проявления зависят от общей физиологической реактивности организма (т. е. его способности вступать во взаимодействие с микроорганизмом и реагировать на него как на фактор, нарушающий нормальные физиологические функции), которая обусловлена:
Ø Состоянием нервной, эндокринной, иммунной и других систем организма.
Ø Полом и возрастом .
Например, во время менструации, беременности и родов женский организм становиться более чувствительным, в частности к стафилококковым и стрептококковым заболеваниям. Устойчивость ко многим инфекционным заболеваниям детей в возрасте до 6 месяцев связана с наличием материнского иммунитета. Лица преклонного возраста больше подвержены инфекционным заболеваниям вследствие инволюции органов иммунной системы.
Ø Наличие соматических заболеваний (болезни сердечно-сосудистой системы, почек, хронические отравления алкоголем, никотином и др.).
Ø Характером питания. Известно, что при недостаточном, неполноценном и нерациональном питании люди чаще подвержены инфекционным заболеваниям.
Ø Физическим и умственным переутомлением , которые связаны с неравномерным распределением рабочего времени и нарушением режима жизни.
Роль факторов внешней среды в развитии инфекционного процесса
Окружающая среда как третий компонент инфекционного процесса влияет на его возникновение и характер течения, оказывая воздействие как на микро-, так и на макроорганизм.
Ø Климатические условия . В различных климатических зонах юга и севера наблюдается разный уровень заболеваемости кишечными инфекциями, дифтерией, скарлатиной, респираторными вирусными инфекциями.
Ø Температура – охлаждение, перегрев снижает резистентность макроорганизма к инфекции.
Ø Солнечный свет благоприятно влияет на организм и в значительной степени повышает резистентность к инфекционным заболеваниям. Однако в ряде случаев длительное и интенсивное облучение сопровождается понижением устойчивости человеческого организма к ряду патогенных микроорганизмов.
Ø Ионизирующая радиация. Повышенные дозы радиации ослабляют защитно-барьерные функции организма и значительно повышают восприимчивость к различным инфекциям.
Ø Экологическая обстановка – загрязнение воды, воздуха, почвы, особенно в крупных городах, приводит к увеличению частоты инфекционных заболеваний.
Ø Санитарно-гигиенические условия труда и быта.
Ø Чрезвычайно важны и социальные факторы внешней среды: стрессовые ситуации в связи с социально-экономическими и военными конфликтами, состояние здравоохранения, доступность квалифицированной медицинской помощи.
2. Механизмы, пути и факторы передачи инфекции
Механизм передачи возбудителя – это эволюционно сложившийся способ перемещения возбудителя от источника инфекции к восприимчивому организму человека или животного.
Механизм передачи возбудителя реализуется через 3 стадии:
Ø Выделение из зараженного организма;
Ø Циркуляция во внешней среде;
Ø Внедрение в очередной восприимчивый организм.
Факторы передачи – элементы внешней среды, обеспечивающие перенос возбудителя от одного организма к другому.
Пути передачи – это способ проникновения возбудителя в восприимчивый макоорганизм.
Таблица 3.1.
Механизмы | Пути | Факторы | Примеры |
Фекально-оральный |
контактно-бытовой |
пищевые продукты грязные руки, предметы домашнего обихода, игрушки |
Брюшной тиф, паратифы Дизентерия |
Аэрогенный | воздушно-капельный воздушно-пылевой | воздух со взвешенными каплями жидкости воздух с частицами пыли | Менингит, корь, грипп, ветряная оспа Туберкулез |
Трансмиссивный | трансмиссивный (через укус) контаминационный (при втирании) | вши, комары, блохи, клещи и др. | Чума, клещевой энцефалит Сыпной тиф, |
Контактный | прямой контакт непрямой (контактный, трансфузионный, артифициальный) | непосредственный контакт предметы больного, кровь, медицинские инструменты | Гонорея, сифилис, ВИЧ-инфекция и другие ЗППП. Столбняк, гепатиты, ВИЧ-инфекция |
Вертикальный | трансплацентарный | через плаценту | Краснуха, врожденный сифилис, ВИЧ-инфекция |
3. Формы инфекции и их характеристика
Таблица 3.2.
Признак | Наименование форм инфекций |
По виду возбудителя | бактериальная вирусная грибковая протозойная |
По происхождению | экзогенная эндогенная (аутоинфекция – как разновидность) |
По локализации возбудителя | местная (очаговая) общая (генерализованная): бактериемия, вирусемия, сепсис, септицемия, септикопиемия, |
По длительности пребывания в организме |
хроническая носительство |
По числу видов возбудителей | моноинфекция смешанная (микст) инфекция |
По наличию симптомов | бессимптомная манифестная персистирующая |
По механизму передачи | кишечные инфекции инфекции дыхательных путей кровяные инфекции заболевания, передающиеся половым путем раневая инфекция |
По источнику инфекции | антропонозы антропозоонозы сапронозы |
По степени распространенности | спородическая заболеваемость эпидемическая вспышка эпидемия пандемия эндемические заболевания экзотическая заболеваемость |
Повторные заболевания | вторичная инфекция реинфекция суперинфекция |
Экзогенная инфекция – инфекция, возникающая в результате заражения человека патогенными микроорганизмами, поступающими из окружающей среды с пищей, водой, воздухом, почвой, выделениями больного.
Эндогенная инфекция – инфекция, вызываемая представителями нормальной микрофлоры – условно-патогенными микроорганизмами самого индивидуума.
Аутоинфекция – разновидность эндогенной инфекции, которая возникает в результате самозаражения путем переноса возбудителя из одного биотопа в другой.
Местная (очаговая) инфекция –микроорганизмы локализуются в местном очаге. Генерализованная инфекция – инфекция, при которой возбудитель распространяется по организму лимфогенным или гематогенным путем.
Бактериемия/вирусемия – распространение возбудителя гематогенным путем, при этом кровь является механическим переносчиком возбудителя, т. к. микроорганизмы в ней не размножаются.
Сепсис – генерализованная форма инфекции, характеризующаяся размножением возбудителя в крови. Выделяют 2 формы сепсиса:
Септицемия (первичный сепсис) – возбудитель сразу из входных ворот попадает в кровь и размножается в ней.
Септикопиемия (вторичный метастатический сепсис) развивается в результате генерализации локального инфекционного процесса и характеризуется возникновением вторичных гнойных очагов во внутренних органах.
Токсико-септический шок (бактериальный) – возникает при массивном поступлении бактерий и их токсинов в кровь.
Моноинфекция вызывается одним видом возбудителя, смешанная – двумя или несколькими.
Острая инфекция протекает в короткие сроки.
Хроническая инфекция характеризуется длительным пребыванием микроорганизмов в организме.
Микробоносительство – своеобразная форма инфекционного процесса, при котором макроорганизм не способен полностью элиминировать микроорганизмы, а микроорганизмы не в состоянии больше поддерживать активность инфекционного заболевания. В зависимости от длительности реконвалесцентное носительство разделяют на: о строе (до 3 месяцев после клинического выздоровления) и хроническое (свыше 3 месяцев).
Бессимптомная инфекция (инаппарантная) характеризуется отсутствием клинических проявлений болезни.
Манифестная инфекция характеризуется наличием характерного симптомокомплекса.
Персистирующая инфекция характеризуется чередованием бессимптомных периодов (ремиссии) с периодами клинических проявлений (обострений, рецидивов).
Раневая инфекция (инфекция наружных покровов) – возбудитель попадает в организм человека или животного через порезы, ссадины и другие травматические повреждения целостности кожных покровов (столбняк, газовая гангрена).
Антропонозы – болезни, при которых только человек является источником инфекции (дифтерия, коклюш, лепра).
Зоонозы – болезни, при которых источником инфекции являются животные (бешенство , туляремия, бруцеллез).
Антропозоонозы – источником инфекции могут быть как животные, так и человек.
Сапронозы – инфекционные болезни, возбудители которых являются свободно-живущими в окружающей среде организмами (легионеллез).
Спородическая заболеваемость – единичные, не связанные между собой заболевания.
Эпидемическая вспышка – групповые заболевания, связанные одним источником инфекции и не выходящие за пределы семьи, коллектива , населенных пунктов.
Эпидемия – широкое распространение инфекционной болезни, охватывающее население региона, страны или нескольких стран.
Пандемия – распространяется во многих странах или даже во всех частях света.
Эндемия – постоянно регистрируемая на определенной территории заболеваемость, обусловленная социальными и природными условиями.
Экзотическая заболеваемость – заболеваемость, несвойственная данной местности, развивается в результате заноса или завоза возбудителя с других территорий.
Вторичная инфекция – к первоначальной болезни присоединяется другая, вызванная новым возбудителем.
Реинфекция – заболевание, возникающее после перенесенной инфекции в случае повторного заражения тем же возбудителем.
Суперинфекция – инфицирование макроорганизма тем же возбудителем еще до выздоровления.
Рецидив – возврат клинических проявлений болезни без повторного заражения за счет оставшихся в организме возбудителей.
4. Периоды инфекционного заболевания
Каждая манифестная инфекция характеризуется определенным симптомокомплексом и циклическим течением болезни, т. е. последовательной сменой отдельных ее периодов, отличающихся продолжительностью, клиническими симптомами, микробиологическими, иммунологическими и эпидемиологическими особенностями.
I . Инкубационный период (скрытый) – промежуток времени проникновения возбудителя в организм и появлением первых клинических симптомов заболевания.
Длительность инкубационного периода различна при разных инфекциях (от нескольких часов до нескольких лет) и даже у отдельных больных, страдающих одним и тем же заболеванием. Она зависит от вирулентности возбудителя и его инфицирующей дозы, локализации входных ворот, состояния организма человека перед заболеванием, его иммунного статуса. Больной не представляет опасности для окружающих, поскольку возбудитель обычно не выделяется из организма человека в окружающую среду.
II . Продромальный (начальный) период – появление неспецифических симптомов заболевания. В данный период возбудитель интенсивно размножается и колонизирует ткань в месте его локализации, а также начинает продуцировать соответствующие ферменты и токсины. Клинические признаки заболевания в этот период не имеют четких специфических проявлений и зачастую одинаковы при разных заболеваниях: повышение температуры тела, головная боль, миалгии и артралгии, недомогание, разбитость, снижение аппетита и т. д. Обычно продолжается от нескольких часов до нескольких дней. При многих инфекционных заболеваниях возбудители в период продромы не выделяются во внешнюю среду (исключение, корь, коклюш и др.).
III. Разгар болезни – появление и нарастанием наиболее характерных, специфичных для конкретного инфекционного заболевания клинических и лабораторных признаков. В начале данного периода обнаруживаются специфические антитела в сыворотке крови больного, титр которых в дальнейшем увеличивается . Возбудитель продолжает интенсивно размножаться в организме, накапливаются значительные количества токсинов и ферментов. Вместе с тем, происходит выделение возбудителя из организма больного , вследствие чего он представляет опасность для окружающих.
IV . Исход заболевания:
Ø выздоровление (реконвалесценция);
Ø микробоносительство;
Ø переход в хроническую форму;
Ø летальный.
Реконвалесценция развивается после угасания основных клинических симптомов. При полном выздоровлении восстанавливаются все функции , нарушенные вследствие инфекционного заболевания. Титр антител достигает максимума . При многих заболеваниях в период реконвалесценции возбудитель выделяется из организма человека в большом количестве.
5. Патогенность, вирулентность, факторы патогенности
Патогенность (от греч. patos – страдание, genos – происхождение) – потенциальная способность микроорганизмов вызывать инфекционный процесс (генетически детерминированный, видовой признак, являющийся качественной характеристикой).
Вирулентность (от лат. virulentus – ядовитый, заразный) – фенотипическое выражение патогенности, т. е. каким образом реализуется патогенность в зависимости от условий (количественная характеристика).
Единицы измерения вирулентности:
D lm ( Dosis letalis minima) – наименьшее количество микроорганизмов, вызывающих не менее 95% гибели лабораторных животных.
Dl50 – летальная доза, вызывающая гибель 50% животных (наиболее объективный критерий).
Dc ( Dosis cerata letalis ) – смертельная доза 100% гибели животных.
Di – инфицирующая доза возбудителя.
Таблица 3.3.
Факторы патогенности микроорганизмов
Структурные и химические компоненты клетки | Ферменты | Токсины |
|
Пили I, II типа Антигены, белки клеточной стенки | Плазмокоагулаза Фибринолизин Гиалуронидаза Лецитиназа Нейраминидаза и др. | Экзотоксины Эндотоксины |
Структурные и химические компоненты клетки:
Ø Капсула защищает от фагоцитоза.
Ø Пили I типа принимают участие в адгезии, пили II типа (конъюгативные) участвуют в передаче генетического материала, в частности в передаче R-плазмиды, отвечающей за множественную лекарственную устойчивость.
Ø Жгутики способствуют быстрому перемещению возбудителя в организме.
Ø Антигены и белки клеточной стенки обладают антифагоцитарным действием.
Ферменты патогенности:
Ø Плазмокоагулаза – способствует выпадению нитей фибрина из плазмы и на поверхности микроорганизма образуется фибриновая пленка, защищающая от фагоцитоза (например, St. aureus).
Ø Фибринолизин – превращает плазминоген крови в фермент, растворяющий сгустки фибрина, что способствует распространению возбудителя из местного ограниченного очага.
Ø Гилуронидаза – расщепляет гиалуроновую кислоту, входящую в состав межклеточного вещества и тем самым повышается проницаемость слизистых оболочек и соединительной ткани.
Ø Лецитиназа – разрушает лецитин, содержащийся в оболочках клеток человека.
Ø Нейраминидаза – расщепляет сиаловую (нейраминовую) кислоту, повышая проницаемость различных тканей.
Ø Коллагеназа – разрушает коллагеновые структуры мышечной ткани, вызывая ее расплавление.
Ø Протеаза – разрушает белки.
Ø Уреаза – гидролизует мочевину с образованием аммиака и СО2 и др.
Токсины :
Бактериальные токсины делятся на экзо - и эндотоксины.
Таблица 3.4.
Сравнительная характеристика экзо - и эндотоксинов
Свойства | Экзотоксины | Эндотоксины |
Основные особенности | Выделяются во внешнюю среду | Прочно связаны со структурами бактериальной клетки |
Продуцент | Преимущественно Гр (+) бактерии | Гр (−) бактерии |
Химическая структура | Липополисахариды клеточной стенки |
|
Чувствительность к температуре | Термолабильны | Термостабильны |
Токсичность | Умеренная |
|
Антигенность | Умеренная |
|
Органотропность | Отсутствует |
|
Действие на организм | Специфическое, избирательное | Неспецифическое: повышение температуры, интоксикация, сосудистые нарушения |
Возможность получения анатоксина | Легко получить при обработке формалином 0,3-0,4%, при 37-400С в течении 30-40 дней (Рамон,1923) | Большинство не переводится в анатоксины |
Классификация экзотоксинов по механизму действия:
Цитотоксины блокируют синтез белка на рибосомах (например, дерматонекротоксин дифтерийной палочки).
Мембранотоксины повышают проницаемость мембраны эритроцитов (гемолизины) и лейкоцитов (лейкоцидины), вызывая гемолиз первых и разрушение вторых (например, α-токсин золотистого стафилококка, О-стрептолизин Str. рyogenes).
Функциональные блокаторы активируют клеточную аденилатциклазу, что приводит к повышению проницаемости стенки тонкой кишки и увеличению выхода жидкости в ее просвет – диарее (холероген холерного вибриона, энтеротоксин E. coli). Функциональные блокаторы (нейротоксины) возбудителей столбняка и ботулизма блокируют передачу нервного импульса.
Эксфолиатины и эритрогенины влияют на процесс взаимодействия клеток между собой и с межклеточным веществом (например, продуцируются St. aureus и Str. рyogenes).
Перечисленные факторы патогенности обуславливают:
Ø Адгезию – процесс прикрепления на клетках хозяина.
Ø Колонизацию – процесс размножения микроорганизмов в месте адгезии, обеспечивает накопление микроорганизмов до такой критической концентрации, которая способна вызвать патологическое действие.
Ø Пенетрацию – проникновение внутрь эпителиальных и других клеток, при этом клетки разрушаются, что сопровождается нарушением целостности эпителиального покрова соответствующего органа и возникновением патологического процесса.
Ø Инвазию – способность проникать через слизистые и соединительнотканные барьеры в подлежащие ткани.
Ø Агрессию – способность противостоять защитным силам макроорганизма и оказывать патогенное токсическое действие.
6. Инфекционные свойства вирусов.
У вирусов на применяют понятия патогенность и вирулентность, а вместо этих понятий используют термин инфекционность .
Инфекционность вирусов обусловлена:
Ø ДНК или РНК вируса.
Ø Белками капсида, которые могут обладать токсичностью;
Ø Способностью образовывать внутриклеточные включения (например, тельца Бабеша-Негри при бешенстве – в цитоплазме клеток ЦНС, тельца Гварниери при оспе – в цитоплазме эпителиальных клеток);
Ø Антигенами суперкапсида: гемагглютинином, нейраминидазой, F-белком слияния.
Особенности вирусных инфекций
Ø Способность вирусов (большинство ДНК-содержащие) встраивать свою нуклеиновую кислоту в хромосому клетки хозяина при отсутствии стадии репродукции, сборки и выхода вируса из клетки, вызывая интегративную инфекцию (вирогению).
Ø Наличие стадии вирусемии , во время которой вирус циркулирует в крови. Исключение – вирусы, распространяющиеся нейрогенным путем (вирусы бешенства, простого герпеса и др.)
Ø Поражение вирусами лимфоцитов (вирусы гриппа, герпеса, полиомиелита и др.), что приводит к возникновению иммунодефицитных и других иммунопатологических состояний.
Ø Образование внутриядерных или внутрицитоплазматических включений , представляющих собой внутриклеточные скопления вируса (имеют диагностическое значение).
Таблица 3.5.
Формы вирусных инфекций
Развитие инфекционного процесса зависит от основных свойств микроорганизма. К этим свойствам относятся патогенность и вирулентность.
Патогенность ― это потенциальная способность микробов вызывать инфекционный процесс. Патогенные микробы оказывают поражающее и токсическое действие на ткани больного организма. Патогенность является генетическим признаком определенного вида микроба и определяется его генотипом. Патогенность характеризуется специфичностью действия микроба.
Вирулентность ― мера, степень патогенности, связанная с индивидуальным свойством штамма, которая меняется в различных условиях среды. Высокая вирулентность обычно характерна для свежевыделенных штаммов микробл, а при сохранении их в лабораторных условиях она постепенно снижается, но не исчезает. В эксперименте вирулентность микроба можно усилить последовательными пассажами через организм восприимчивых животных. Например, вирулентность стрептококка возрастает при многократных пассажах через организм белых мышей. В классическом опыте Пастер резко усилил вирулентность вируса бешенства для кроликов путем последовательного пассирования через мозг кроликов.
Создавая неблагоприятные условия для жизнедеятельности патогенного микроба путем воздействия физических, химических и биологических факторов, можно ослабить его вирулентность. К этим факторам относятся: повышенная температура (Пастер стойко ослабил вирулентность возбудителя сибирской язвы при температуре 43°), антимикробные препараты, иммунные сыворотки, пересевы на различные питательные среды.
Объективным показателем вирулентности патогенных микробов в естественных условиях является тяжесть и исход вызываемого ими заболевания, а в лаборатории ― количество (доза), вызывающее гибель или инфицирование подопытных животных. Установлено наиболее верным определение 50% летальной (LD50) или инфицирующей (ID50) дозы. Патогенность рассматривается в органической связи с вирулентностью и характеризуется тремя неотъемлемыми свойствами микроорганизмов: инфективностыо, инвазн-онностью и токсигенностью (В. Д. Тимаков, В. Г. Петровская).
Инфективность (заразительность) ― способность патогенного микроба вызывать инфекционный процесс в естественных условиях. Для инфективности характерны способность микроба выживать во внешней среде и проникать через естественные барьеры, т. е. переходить от больного организма к здоровому.
Инвазионность―способность патогенного микроба преодолевать защитные механизмы организма с целью поражения естественно избранного им органа, где он находит благоприятные условия для активного размножения и количественного накопления. Микробы, обладающие инвазионными свойствами, вызывают на месте их внедрения в организм изменение ткани. Вещества, изменяющие проницаемость местной ткани, называются инвазинами, или факторами распространения. Было установлено, что такое вещество (гиалуронидаза) обнаруживается в фильтратах бульонных культур различных видов микроорганизмов. Инвазионность осуществляется целым арсеналом средств. К ним относятся: гиалуронидаза, капсулообразование, капсульные антигены, агрессины, антифагины.
Гиалуронидаза относится к ферментам патогенности и оказывает разрушающее действие на гиалуроновую кислоту (по-лисахаридное образование соединительной ткани), которая создает препятствие проникновению и распространению микробов в организме. Выявление этого фермента основано на его способности гидролизовать гиалуроновую кислоту, которая теряет способность образовать с уксусной кислотой сгусток муцина.
К а п су л о о б р а з о в а н и е ―вирулентность некоторых видов микробов (пневмококки, сибиреязвенные бактерии и др.) связана с их способностью образовывать капсулы в организме человека и животных. Капсула сибиреязвенной бактерии обладает выраженной антифагоцитарной активностью, т. е. защищает бактерии от действия фагоцитоза. Это было доказано опытом. Если морской свинке ввести смесь капсульной и бескапсульной культур сибиреязвенных бацилл, то фагоцитозу подвергаются только бескапсуль-ные, а капсульные развиваются и размножаются в организме.
Капсульные антигены. Патогенные бактерии содержат поверхностные антигенные компоненты, подавляющие защитные функции макроорганизма. Такими свойствами обладают полисаха-ридные антигены пневмококков, vi-антиген энтеробактерий, М-протеин гемолитических стрептококков и др. Антиген типа vi обнаружен у возбудителя туляремии.
Агрессины ― вещества, подавляющие защитные функции организма, были обнаружены у возбудителей чумы, дифтерии, сибирской язвы, брюшного тифа, паратифов, туберкулеза, а также у пневмококков, стафилококков и стрептококков. Агрессины были получены Байлем при фильтрации экссудата из плевральной полости подопытных животных, зараженных возбудителем сибирской язвы и пневмококками. Сам фильтрат не опасен, но если добавить его к несмертелыюй дозе соответствующего микроба, то это вызывает смертельное заболевание с последующей гибелью лабораторных животных.
Антифагины ― вещества, выделенные из взвеси различных видов микроорганизмов, обладающие способностью подавлять фагоцитоз. Они разрушаются при кипячении в течение 20 минут.
К веществам, определяющим вирулентность микроорганизмов, относятся и химические компоненты. Их молено использовать для дифференциации патогенных микробов от непатогенных. Например, штамм микобактерий туберкулеза (Н = 37 RV), обладающий высокой вирулентностью, содержит 7,6% липополисахаридов и фракцию, состоящую из миколовой кислоты (65―80%), авирулентный штамм (Н = 37 Ra) содержит только 0,5% липополисахаридов и не имеет миколовой кислоты. Выявлена существенная разница в количестве рибонуклеиновой и дезоксирибопуклеиновой кислот у холерного и холероподобиого вибрионов (соответственно 1: 9 и 1:1). Такие данные были обнаружены у некоторых патогенных и пепатогенных микроорганизмов.
Токсигенность ― это способность микроорганизма нарушать метаболические функции макроорганизма. Токсипообразование для некоторых видов микробов является жизненно необходимым процессом. Ядовитые вещества, вызывающие патологические изменения в клетках, тканях и органах макроорганизма, называются токе и нам и.
По характеру образования микробные токсины подразделяются на экзотоксины и эндотоксины.
Экзотоксины выделяются возбудителями газовой анаэробной инфекции, ботулизма, столбняка, дифтерии, дизентерийными бактериями Григорьева―Шига, а также отдельными видами стафилококков и гемолитических стрептококков. Они являются сильными биологическими ядами и в минимальных дозах действуют на чувствительных животных.
Дифтерийный токсин вызывает некроз тканей в зоне внедрения возбудителя и распространяется по всему организму, в котором поражает мышечные, нервные, печеночные, почечные, кожные и другие ткани. Столбнячный токсин действует на двигательные клетки передних рогов спинного мозга и вызывает судорожные мышечные сокращения у восприимчивого организма. Экзотоксины у возбудителей дифтерии, столбняка и газовой анаэробной инфекции разрушаются под воздействием пищеварительных ферментов, а у патогенных стафилококков п палочек ботулизма не разрушаются в желудке и кишечнике. Они вызывают отравление при пероральном введении в организм.
Сила действия микробных токсинов определяется путем их введения в организм восприимчивых животных по принятой методике (Dim, Dl50). За единицу измерения силы дифтерийного токсина принимается 1 Dim, т. е. минимальное количество токсина, которое при подкожном введении морским свинкам весом в 250 г приводит их к гибели на четвертые сутки. Минимальная смертельная доза нативного дифтерийного токсина для морской свинки ― 0,002 мл, столбнячного токсина для белой мыши ― 0,000005 мл, ботулиниче-ского токсина для морской свинки ― 0,00001―0,000001 мл.
Экзотоксины, полученные в очищенном виде, обладают высокой токсичностью для восприимчивых животных. 1 мг азота кристаллического столбнячного токсина содержит 50―75x10", ботули-нического ― 220ХЮ6 Dim для белых мышей и дифтерийного ― 50000―60000 Dim для морских свинок.
Получение экзотоксинов. Токсин получают из питательных сред, в которых культивируются продуценты экзотоксинов, путем их фильтрования. Фильтрат, содержащий экзотоксин, не может считаться чистым токсином, ибо в нем содержатся вещества, входящие в состав питательной среды, и различные продукты обмена. Поэтому проводят очистку и концентрацию токсинов путем применения методов коагуляции в изоэлектрической точке, высаливания сульфатом аммония, многократного переосаждения трихлоруксус-ной кислотой при низкой температуре и рН около 4,0, а также адсорбции различными веществами.
Эндотоксины образуются многими видами микроорганизмов. Например, возбудители брюшного тифа, паратифов А и В, дизентерии, Менингита, гонореи и другие патогенные грамотрицательные бактерии содержат эндотоксины. Они находятся внутри клетки и прочно связаны с телами бактерии. Эндотоксины вызывают в организме комплекс патологических изменений, главным образом действуют на эндотелий капилляров, лейкоциты, лимфо-идную ткань и вегетативную нервную систему. Они освобождаются из клеток при разрушении их ультразвуком, повторным замораживанием и оттаиванием, при экстрагировании слабыми кислотами и щелочами. Например, эндотоксин у дизентерийной бактерии Григорьева―Шига получают путем разрушения клеток и осаждения белков трихлоруксусной или соляной кислотой с последующим центрифугированием.
По химическому составу и некоторым другим признакам токсины делятся на следующие.
Токсины белковой природы ― это экзотоксины, выделяющиеся в питательную среду. Химический состав экзотоксина сложный. Например, дифтерийный экзотоксин имеет общий азот ― 16%, аминный азот ―0,98%, серу ―0,75%, фосфор ― 0,05%. Экзотоксины разрушаются при температуре 60―80° в течение 20―50 минут, при кипячении ― моментально. У экзотоксинов обнаружено явление потенсирования, т. е. смесь токсинов действует на организм более ядовито, чем монотоксин. Резко выражено по-тенсирующее действие токсинов у возбудителей столбняка, газовой анаэробной инфекции и стафилококков, а также возбудителя дифтерии.
Токсины, относящиеся к глюцидо-липидно-про-теиновым комплекса м,― это эндотоксины, связанные с телами грамотрицательных бактерий (кишечно-тифознс-дизентерийная группа, бруцеллы, менингококки). Их не бывает у грамположн-тельных бактерий. Химический состав токсинов: полисахариды (50―65%), жирные кислоты (20―25%), уксусная и фосфорная кислоты, а также протеины и азотистые соединения.
Полисахаридные токсины. Это токсические вещества, выделяемые из бактерий, представляющие собой специфические полисахариды, отличающиеся от обычных полисахаридов содержанием в своем составе глюкозы, галактозы, арабинозы, маннозы, рамнозы, аминосахаридов, липидов и других веществ. Полисахаридные токсины обладают гемолитическими, лейкотоксическими и нейротропными свойствами.
Ферменты патогенности. Токсины играют ведущую роль в патогенезе инфекционных болезней, но не единственную. Их токсическое действие осуществляется в комплексе с ферментами, названными в литературе «ферментами патогенности», и продуктами распада клеток и тканей. Они вызывают не только очаговые поражения, но и через нейро-гуморальную систему нарушения функции различных органов. В результате этого угнетаются защитные механизмы организма, происходит количественное накопление и активное действие возбудителей инфекционных заболеваний.
Обитая в инфицированном организме человека, патогенные бактерии совершают сложные биохимические процессы, катализируемые ферментными системами. Вырабатываемые ими продукты обмена, включая и продукты аутолиза бактерий, нарушают взаимные связи и согласованность действий различных органов и систем в динамике болезни. По характеру влияния на патогенез болезни ферменты патогенности подразделяются на 4 группы: первая ―обладает высокой токсичностью; вторая, не обладая токсичностью,― переводит протоксин в токсин с многократным усилением его ядовитости; третья ― способствует распространению бактерий и их токсинов В тканях; четвертая ― вызывает образование в организме неспецифических ядовитых продуктов клеточного распада.
Ферменты (гиалуронидаза, коагулаза, стрептокиназа и др.) подавляют защитные механизмы организма и усиливают вирулентность у патогенных бактерий. Лейкоцидин стафилококков вызывает гибель нейтрофилов крови; декарбоксилазы аминокислот, синтезируемые бактериями кишечной группы, защищают их от действия кислой среды. По химической структуре ферменты патогенности близки к токсинам. Они взаимодействуют между собой и являются оружием патогенных микробов.
Похожая информация.
Инфекционная доза, которая для человека не установлена, и серьезность конечной инфекции явно зависят от нескольких факторов, таких как путь заражения, истощение и другие аспекты состояния здоровья инфицированного и, вероятно, от относительной вирулентности инфицирующего штамма. При оценке риска неизбежна зависимость от информации о тестах на животных. Опубликованные данные по инфицирующей и летальной дозе для животных переносятся и на человека (Watson and Keir, 1994).
Кожная инфекция. Для начала кожной инфекции, по-видимому, не требуется большого количества спор, но споры должны проникнуть в субэпидермальные ткани через порез или ранку. Риск заражения значительно снижается при использовании на опасных работах соответствующей одежды и перчаток, перевязкой ран и другими гигиеническими мерами.
Легочная (ингаляционная) инфекция. Зарегистрированная LD50 у нечеловеческих приматов составляет от 2 500 до 760 000 спор (Meselson et al., 1994; Watson and Keir, 1994). US Department of Defence основывает свои стратегические планы, исходя из LD50 для человека, равной 8 000 - 10 000 спор (Meselson et al., 1994). Тем не менее единственными строго определенными данными по ингаляционной инфицирующей дозе для человека являются данные, полученные в ходе исследовании на фабриках по переработке козьей шерсти, приведенные ранее. В любом случае, для того, чтобы риск легочной сибирской язвы стал значительным, очевидно необходима существенная экспозиция. В недавних исследованиях (Turnbull et al., 1998) наибольшие уровни в пробах воздуха от 3 до 9 м по ветру от disturbed dry сухой остаток the highest levels found in air sampled 3 to 9 m downwind from disturbed dry, dusty anthrax carcass sites in Namibia were 20 to 40 colony forming units of spores per cubic metre.
Это соответствует сдержанным оценкам о том, что обычному человеку, проявляющему умеренную активность, требуется около 2,5 мин., чтобы вдохнуть одну спору. Более того, установлено, что при размерах частиц более 5 µm они достигают альвеол легких с возрастающими трудностями. Следовательно, вероятность того, что вдыхаемые споры проникнут внутрь достаточно глубоко, чтобы индуцировать легочную форму сибирской язвы, сильно зависит от размеров частиц, к которым споры прикреплены.
Следовательно, риск заболевания легочной формой сибирской язвы вне промышленных условий чрезвычайно низок.
Оральный путь инфекции. Информации об инфекционной дозе через оральные ворота очень мало, однако то, что верно для кожных покровов, в большой степени справедливо и для орофарингеального и гастроинтестинального эпителия. Вероятность инфицирования, очевидно, значительно увеличивается, если не прямо зависит от того, есть ли пораженные участки эпителия, через которые споры могу проникнуть внутрь и дать начало инфекции.
При оценке риска необходимо также учитывать тот факт, что сибирская язва хорошо поддается лечению, если диагноз установлен на ранних стадиях болезни. Сведения о возможной экспозиции также являются важной составляющей для стабилизации положения.
Таким образом, можно выделить главные эпизоотологические критерии сибирской язвы.
1. Восприимчивые животные. Сибирской язвой болеют крупный рогатый скот, овцы, козы, лошади, олени, верблюды, буйволы, свиньи. Этот список пополнили представители многих видов диких животных: слоны, водяные и африканские буйволы, лесные бизоны, белохвостые олени, антилопы-куду, лошадиная антилопа, лесная антилопа (дукер), антилопа импала, антилопа канна, стенбоки, зебры Бурчелла, бегемоты, болотные козлы, страусы, хорьки, ослы. В 1996 году появилось сообщение о заболевании диких гиеновых собак (Coper J.E.,1996). 36 видов африканских диких животных погибают от антракса.
2. Источники возбудителя инфекции и факторы его передачи. Наибольшую опасность представляют больные животные, выделяющие возбудитель во внешнюю среду. Огромную опасность представляют места гибели или захоронения павших от сибирской язвы животных, неубранные трупы, которые растаскивают хищники. Установлено, что наиболее высокая концентрация спор Bac. Anthracis отмечена вокруг трупа в радиусе до 5 метров (до 10 5 спор на 1 г почвы). В фекалиях гиен также высокая концентрация возбудителя, т.к. они поедают трупы павших от антракс животных. Ниже концентрация спор в фекалиях грифов, которые питаются на более свежих трупах. У львов, гиен и шакалов обнаружен высокий титр антител к протективному сибиреязвенному антигену (Lindeque P.M.,1996).
Занос сибирской язвыв благополучные страны чаще всего происходит с инфицированным мясом и мясными продуктами, а также с костной мукой. Такие случаи отмечены в Норвегии, Непале, Индонезии и т.д.
Подчеркивается роль насекомых (членистоногих) как переносчиков возбудителя антракс особенно на территории Индии и Канады.
3. Стационарность сибирской язвы. Это наиболее яркая эпизоотологическая особенность сибирской язвы. В ранее неблагополучных пунктах спустя многие десятилетия полного благополучия вновь возникали случаи сибирской язвы. Как правило, это связано со стихийными бедствиями (наводнениями, землетрясениями, оползнями, пыльными бурями и т.п.), а также с проведением различного вида земляных, строительных и мелиоративных работ. Отмечены вспышки антракса в Австралии и США на трассах перегона скота спустя не менее ста лет после первых зарегистрированных случаев. Ранее инфицированные пастбища многие десятилетия сохраняют опасность.
4. Сезонность болезни. Периодичность. Особой закономерности в проявлении сибирской язвы не просматривается, интервалы между крупными эпизоотиями составляют в разных регионах 3-5 лет и более.Сезонность просматривается довольно четко, но зависит от географии болезни, от климатических, а иногда и хозяйственных условий. Как правило, вспышки регистрируются чаще в теплое время года. Инцидентность повышается в условиях засухи.
5. Особенности процесса в современных условиях. Благодаря налаженному контролю за этой инфекцией, системе мероприятий с применением высокоэффективных средств профилактики эпизоотический процесс характеризуется лишь проявлением спорадических, единичных случаев. В ряде случаев благополучие достигается широкомасштабной вакцинацией животных. Однако сохраняются регионы, где наблюдаются эпизоотии антракс, особенно часто среди свободно живущих диких животных.
Благодаря наличию споровых форм, бактерия сибирской язвы всегда рассматривалась как объект разработок биологического оружия массового поражения. При наличии соответствующих погодных условий, 50 килограмм сибириязвенных спор, распыленных с самолета, могут покрыть территорию в 20 квадратных километров, при этом (благодаря маленьким размерам спор) будут поражены все жители независимо от того, находятся ли они в помещении или на улице. По расчетам ВОЗ, на каждые 5 млн. случаев пораженной таким образом популяции будет 250 тыс. заболевших и до 100 тыс. жертв. По оценкам американских военных достаточно лишь 100 килограмм спор для того, чтобы биотеррористы смогли убить до 3 млн. человек в г.Вашингтоне, округ Колумбия.Иллюстрацией опасности сибирской язвы может послужить последний случай массового заражения легочной формой, который имел место в России в 1979 г., в Свердловске, где заболело 79 человек, 68 из которых погибли.
Ещё во время второй мировой войны остров Gruinard был местом первого научного испытания Bac.anthracis в качестве потенциального агента биологического оружия.
Испытания подтвердили, что жизнеспособные споры антракса можно с помощью взрыва рассеивать в виде облака, которое вызывало летальное поражение при вдыхании чувствительными млекопитающими. Более чем через 20 лет большое количество жизнеспособных высоковирулентных спор было обнаружено в почве. В 1986 году проведена деконтаминация почвы с предварительным сжиганием растительности. Формальдегид растворяли в морской воде. Наиболее эффективным оказалось использование 5%-го раствора формальдегида из расчета 50 литровкв.м. Через 2 месяца были взяты пробы почвы. В 9 местах обнаружены споры возбудителя. Эти участки были повторно обработаны формальдегидом посредством поверхностной ирригации. В октябре 1987 года споры антракса в этих местах не были обнаружены.
Учение об инфекционных болезнях уходит в глубь веков. Представление о заразности таких болезней, как чума, оспа, холера и многие другие, зародилось еще у древних народов; задолго до нашей эры уже применялись некоторые простейшие меры предосторожности в отношении заразных больных. Однако эти отрывочные наблюдения и смелые догадки были весьма далеки от подлинно научных знаний.
Уже в Древней Греции некоторые философы, например Фукидид, высказывали мысль о живых возбудителях («контагиях») инфекционных болезней, но эти ученые не имели возможности подтвердить свои предположения какими-либо достоверными фактами.
Выдающийся врач древнего мира Гиппократ (около 460- 377 гг. до н. э.) объяснял происхождение эпидемий действием «миазм» - заразных испарений, которые будто бы могут вызвать ряд болезней.
Передовые умы человечества даже в условиях средневековой схоластики справедливо отстаивали идею о живой природе возбудителей заразных болезней; например, итальянский врач Фракасторо (1478-1553) развил стройное учение о контагиях болезней и о способах их передачи в своем классическом труде «О контагиях и контагиозных болезнях» (1546).
Голландский естествоиспытатель Антоний ван Левенгук (1632-1723) сделал в конце XVII века весьма важное открытие, обнаружив под микроскопом (который был им лично изготовлен и давал увеличение до 160 раз) различные микроорганизмы в зубном налете, в застоявшейся воде и настое из растений. Свои наблюдения Левенгук описал в книге «Тайны природы, открытые Антонием Левенгуком». Но даже и после этого открытия идея о микробах как возбудителях инфекционных болезней долгое время не получала еще необходимого научного обоснования, хотя опустошительные эпидемии неоднократно развивались в различных странах Европы, унося тысячи человеческих жизней.
На протяжении многих десятилетий (в XVII и XVIII столетиях) наблюдения над эпидемиями инфекционных болезней, поражающими большое количество людей, убеждали в заразности этих заболеваний.
Исключительно важное практическое значение имели работы английского ученого Эдуарда Дженнера (1749-1823), разработавшего высокоэффективный метод прививок против натуральной оспы.
Выдающийся отечественный врач-эпидемиолог Д. С. Самойлович (1744-1805) доказал заразность чумы при близком соприкосновении с больным и разработал простейшие способы дезинфекции при этом заболевании.
Великие открытия французского ученого Луи Пастера (1822-1895) убедительно доказали роль микроорганизмов в процессах брожения и гниения, в развитии инфекционных болезней.
Работы Пастера объяснили действительное происхождение инфекционных болезней человека, они явились экспериментальной основой асептики и антисептики, блестяще разработанных в хирургии Н. И. Пироговым, Листером , а также их многочисленными последователями и учениками.
Огромной заслугой Пастера явилось открытие принципа получения вакцин для предохранительных прививок против инфекционных болезней: ослабление вирулентных свойств возбудителей путем особого подбора соответствующих условий для их культивирования. Пастером были получены вакцины для прививок против сибирской язвы и бешенства.
Немецкий ученый Леффлер доказал в 1897 г. принадлежность возбудителя ящура к группе фильтрующихся вирусов.
Необходимо отметить, что вплоть до середины прошлого века многие инфекционные болезни, носившие название «лихорадок» и «горячек», совершенно не дифференцировали. Лишь в 1813 г. французский врач Бретанно высказал предположение о самостоятельности заболевания брюшного тифа, а в 1829 г. Шарль Луи дал весьма детальное описание клиники этой болезни.
В 1856 г. из группы «горячечных болезней» были выделены брюшной и сыпной тифы с четкой характеристикой этих совершенно самостоятельных заболеваний. С 1865 г. стали признавать отдельной формой инфекционного заболевания и возвратный тиф.
Мировая наука по достоинству оценивает заслуги известного русского клинициста-педиатра Н. Ф. Филатова ( 1847- 1902), внесшего существенный вклад в изучение детских инфекционных болезней, а также
Д. К. Заболотного (1866- 1929), который провел ряд важных наблюдений в области эпидемиологии особо опасных болезней (чума, холера).
В работах нашего соотечественника Н. Ф. Гамалеи (1859- 1949) нашли отражение многие вопросы инфекции и иммунитета.
Благодаря работам И. И. Мечникова (1845-1916) и ряда других исследователей с 80-х годов прошлого века стали получать разрешение вопросы иммунитета (невосприимчивости) при инфекционных болезнях, была показана исключительно важная роль клеточной (фагоцитоз) и гуморальной (антитела) защиты организма.
Помимо чисто клинического исследования инфекционных больных, для диагностики отдельных заболеваний с конца XIX века стали широко применять лабораторные методы.
Работы ряда ученых (И. И. Мечников, В. И. Исаев, Ф. Я. Чистович, Видаль, Уленгут) позволили еще в конце прошлого столетия использовать серологические исследования (агглютинацию, лизис, преципитацию) для лабораторной диагностики инфекционных болезней.
X. И. Гельману и О. Кальнингу принадлежит честь разработки метода аллергической диагностики сапа (1892). Распознавание малярии было значительно облегчено благодаря методу дифференциальной окраски ядра и протоплазмы малярийного плазмодия в мазках крови, разработанному Д. Л. Романовским (1892).
Смысл слова «инфекция» различен. Под инфекцией понимают заразное начало, т.е. возбудителя в одном случае, а в другом случае это слово употребляется как синоним понятия «заражение, или заразная болезнь». Чаще всего слово «инфекция» употребляется для обозначения инфекционной болезни. Инфекционные болезни имеют следующие отличительные особенности:
1) причина - живой возбудитель;
2) наличие инкубационного периода, который зависит от вида микроба, дозы и др. Это период времени от проникновения возбудителя в организм хозяина, его размножение и накопление до предела, обуславливающего болезнетворное действие его на организм (длится от нескольких часов до нескольких месяцев);
3) заразительность, т.е. способность возбудителя передаваться от больного животного здоровому (есть и исключения - столбняк, злокачественный отек);
4) специфические реакции организма;
5) невосприимчивость после переболевания.
Инфекция (позднелатинское infektio - заражение, от латинского inficio - вношу что-либо вредное, заражаю) - состояние зараженности организма; эволюционно сложившийся комплекс биологических реакций, возникающих при взаимодействии организма животного и возбудителя инфекции. Динамика этого взаимодействия называется инфекционным процессом.
Инфекционный процесс - это комплекс взаимных приспособительных реакций на внедрение и размножение патогенного микроорганизма в макроорганизме, направленный на восстановление нарушенного гомеостаза и биологического равновесия с окружающей средой.
Современное определение инфекционного процесса включает взаимодействие трех основных факторов –
1) возбудителя,
2) макроорганизма
3) окружающей среды,
Каждый фактор может оказывать существенное влияние на результат инфекционного процесса.
Чтобы вызвать заболевание, микроорганизмы должны быть патогенными (болезнетворными).
Патогенность микроорганизмов - это генетически обусловленный признак, который передается по наследству. Для того чтобы вызвать инфекционную болезнь, патогенные микробы должны проникать в организм в определенной инфицирующей дозе (ИД). В естественных условиях для возникновения инфекции патогенные микробы должны проникать через определенные ткани и органы организма. Патогенность микробов зависит от многих факторов и подвержена большим колебаниям в различных условиях. Патогенность микроорганизмов может снижаться или, наоборот, увеличиваться. Патогенность как биологический признак бактерий реализуется через их три свойства :
· инфекциозность,
· инвазивность и
· токсигенность.
Под инфекциозностью (или инфективностью) понимают способность возбудителей проникать в организм и вызывать заболевание, а также способность микробов передаваться с помощью одного из механизмов передачи, сохраняя в этой фазе свои патогенные свойства и преодолевая поверхностные барьеры (кожу и слизистые). Она обусловлена наличием у возбудителей факторов, способствующих его прикреплению к клеткам организма и их колонизации.
Под инвазивностью понимают способность возбудителей преодолевать защитные механизмы организма, размножаться, проникать в его клетки и распространяться в нем.
Токсигенность бактерий обусловлена выработкой ими экзотоксинов. Токсичность обусловлена наличием эндотоксинов. Экзотоксины и эндотоксины обладают своеобразным действием и вызывают глубокие нарушения жизнедеятельности организма.
Инфекциозные, инвазивные (агрессивные) и токсигенные (токсические) свойства относительно не связаны друг с другом, они по-разному проявляются у разных микроорганизмов.
Инфицирующая доза - минимальное количество жизнеспособных возбудителей, необходимых для развития инфекционной болезни. От величины инфицирующей дозы микроба может зависеть тяжесть течения инфекционного процесса, а в случае условно-патогенных бактерий - возможность его развития.
Степень патогенности или болезнетворности микроорганизмов называется вирулентностью.
Величина инфицирующей дозы в большой мере зависит от вирулентных свойств возбудителя. Между этими двумя характеристиками существует обратная зависимость: чем выше вирулентность, тем ниже инфицирующая доза, и наоборот. Известно, что для такого высоковирулентного возбудителя, как чумная палочка (Yersinia pestis), инфицирующая доза может колебаться от одной до нескольких микробных клеток; для Shigella dysenteriae (палочка Григоръева-Шига) - около 100 микробных клеток.
В отличие от этого, инфицирующая доза низковирулентных штаммов может быть равна 10 5 -10 6 микробных клеток.
Количественными характеристиками вирулентности являются:
1) DLM (минимальная летальная доза) – доза, вызывающая за фиксированный период времени гибель единичных, наиболее чувствительных подопытных животных; принимается за нижний предел
2) LD 50 – это количество бактерий (доза), вызывающее за фиксированный период времени гибель 50 % животных в эксперименте;
3) DCL (смертельная доза) вызывает за фиксированный период времени
100 %-ную гибель животных в эксперименте.
По степени патогенности они делятся на:
Высокопатогенные (высоковирулентные);
Низкопатогенные (низковирулентные).
Высоковирулентные микроорганизмы вызывают заболевание в нормальном организме, низковирулентные - только в иммуносупрессированном организме (оппортунистические инфекции).
У патогенных микроорганизмов вирулентность обусловлена факторами:
1) адгезия – способность бактерий прикрепляться к эпителиальным клеткам. Факторами адгезии являются реснички адгезии, адгезивные белки, липополисахариды у грамотрицательных бактерий, тейхоевые кислоты у грамположительных бактерий, у вирусов – специфические структуры белковой или полисахаридной природы; Эти структуры, ответственные за прилипание к клеткам хозяина, называются «адгезинами». При отсутствии адгезинов инфекционный процесс не развивается;
2) колонизация – способность размножаться на поверхности клеток, что ведет к накоплению бактерий;
4) пенетрация – способность проникать в клетки;
5) инвазия – способность проникать в подлежащие ткани. Эта способность связана с продукцией таких ферментов, как
- нейраминидаза - фермент, который расщепляет биополимеры, которые входят в состав поверхностных рецепторов клеток слизистых оболочек. Это делает оболочки доступными для воздействия на них микроорганизмов;
· гиалуронидаза - действует на межклеточное и межтканевое пространство. Это способствует проникновению микробов в ткани организма;
· дезоксирибонуклеаза (ДНКаза) - фермент, который деполимеризирует ДНК, и др.
6) агрессия – способность противостоять факторам неспецифической и иммунной защиты организма.
К факторам агрессии относят:
· вещества разной природы, входящие в состав поверхностных структур клетки: капсулы, поверхностные белки и т. д. Многие из них подавляют миграцию лейкоцитов, препятствуя фагоцитозу;капсулообразование - это способность микроорганизмов образовывать на поверхности капсулу, которая защищает бактерии от клеток фагоцитов организма хозяина (пневмококки, чума, стрептококки). Если капсул нет, то образуются другие структуры: например, у стафилококка - белок А, с помощью этого белка стафилококк взаимодействует с иммуноглобулинами. Такие комплексы препятствуют фагоцитозу. Или же микроорганизмы вырабатывают определенные ферменты: например, плазмокоагулаза приводит к свертыванию белка, который окружает микроорганизм и защищает его от фагоцитоза;
· ферменты – протеазы, коагулазу, фибринолизин, лецитиназу;
· токсины, которые делят на экзо– и эндотоксины.
Экзотоксины - это вещества белковой природы, выделяемые во внешнюю среду живыми патогенными бактериями.
Экзотоксины высокотоксичны, обладают выраженной специфичностью действия и иммуногенностью (в ответ на их введение образуются специфические нейтрализующие антитела).
По типу действия экзотоксины делятся на:
А. Цитотоксины - блокируют синтез белка в клетке (дифтерия, шигеллы);
Б. Мембранотоксины - действуют на мембраны клеток (лейкоцидин стафилококка действует на мембраны клеток фагоцитов или стрептококковый гемолизин действует на мембрану эритроцитов). Наиболее сильные экзотоксины вырабатывают возбудители столбняка дифтерии, ботулизма. Характерной особенностью экзотоксинов является их способность избирательно поражать определенные органы и ткани организма. Например, экзотоксин столбняка поражает двигательные нейроны спинного мозга, а дифтерийный экзотоксин поражает сердечную мышцу и надпочечники.
Для профилактики и лечения токсинемических инфекций применяются анатоксины (обезвреженные экзотоксины микроорганизмов) и антитоксические сыворотки.
Рис. 2. Механизм действия бактериальных токсинов. А. Повреждение клеточных мембран альфа-токсином S. aureus. В. Ингибирование белкового синтеза клетки шига-токсином. С. Примеры бактериальных токсинов, активирующих пути вторичных мессенджеров (функциональные блокаторы).
Эндотоксины - токсические субстанции, входящие в структуру бактерий (обычно в клеточную стенку) и высвобождающиеся из них после лизиса бактерий.
Эндотоксины не обладают таким выраженным специфическим действием, как экзотоксины, а также менее ядовиты. Не переходят в анатоксины. Эндотоксины являются суперантигенами, они могут активизировать фагоцитоз, аллергические реакции. Эти токсины вызывают общее недомогание организма, их действие не отличается специфичностью.
Независимо от того, от какого микроба получен эндотоксин, клиническая картина однотипна: это, как правило, лихорадка и тяжелое общее состояние.
Выброс эндотоксинов в организм может привести к развитию инфекционно-токсического шока. Он выражается в потере капиллярами крови, нарушении работы центров кровообращения и, как правило, приводит к коллапсу и смерти.
Различают несколько форм инфекции :
· Выраженной формой инфекции является инфекционная болезнь с определенной клинической картиной (явная инфекция).
· При отсутствии клинических проявлений инфекции ее называют скрытой (бессимптомной, латентной, инапарантной).
· Своеобразная форма инфекции - несвязанное с предшествующим переболеванием микробоносительство.
Возникновение и развитие инфекции зависит от наличия специфического возбудителя (патогенного организма), возможности его проникновения в организм восприимчивого животного, условий внутренней и внешней среды, определяющих характер взаимодействия микро - и макроорганизма.
Каждый вид патогенных микробов вызывает определенную инфекцию (специфичность действия ). Проявление инфекции зависит от степени патогенности конкретного штамма возбудителя инфекции, т.е. от его вирулентности, которая выражается токсигенностью и инвазивностью.
В зависимости от характера возбудителя различают
· бактериальную,
· вирусную,
· грибковую
· другие инфекции.
Входные ворота инфекции – место проникновения возбудителя в организм человека через определенные ткани, лишенные физиологической защиты против конкретного вида возбудителя.
Ими могут быть кожа, конъюнктива, слизистые оболочки пищеварительного тракта, дыхательных путей, мочеполового аппарата. Некоторые микробы проявляют патогенное действие лишь при проникновении через строго определенные ворота инфекции. Например, вирус бешенства вызывает болезнь лишь при внедрении через повреждения кожи и слизистых оболочек. Многие микробы приспособились к разнообразным путям внедрения в организм.
Очаг инфекции (очаговая инфекция) – размножение возбудителя в месте внедрения
В зависимости от механизма передачи возбудителя различают
· алиментарные,
· респираторные (аэрогенные, в т.ч. пылевые и воздушно-капельные),
· раневые,
· контактные инфекции.
При распространении микробов в организме развивается генерализованная инфекция .
Состояние, при котором микробы из первичного очага проникают в кровяное русло, но не размножаются в крови, а лишь транспортируются в различные органы, называется бактериемией . При ряде болезней (сибирская язва, пастереллезы и др.) развивается септицемия : микробы размножаются в крови и проникают во все органы и ткани, вызывая там воспалительные и дистрофические процессы.
Инфекция может быть
· спонтанной (естественной) и
· экспериментальной (искусственной).
Спонтанная инфекция возникает в естественных условиях при реализации механизма передачи, свойственного данному патогенному микробу, или при активизации условно патогенных микроорганизмов, обитавших в организме животного (эндогенная инфекция или аутоинфекция ). Если специфический возбудитель проникает в организм из окружающей среды, говорят об экзогенной инфекции .
Если после перенесения инфекции и освобождения макроорганизма от ее возбудителя происходит повторное заболевание вследствие заражения тем же патогенным микробом, говорят о реинфекци и.
Отмечают и суперинфекцию -следствие нового (повторного) заражения, наступившего на фоне уже развивавшейся болезни, вызванной тем же патогенным микробом.
Возврат болезни, повторное появление ее симптомов после наступившего клинического выздоровления называется рецидивом . Он наступает при ослаблении сопротивляемости животного и активизации сохранившихся в организме возбудителей перенесенной болезни. Рецидивы свойственны болезням, при которых формируется недостаточно прочный иммунитет.
Смешанные инфекции (микстинфекции, миксты ) развиваются в результате заражения несколькими видами микроорганизмов; подобные состояния характеризует качественно иное течение (обычно более тяжёлое) по сравнению с моноинфекцией, а патогенный эффект возбудителей не имеет простого суммарного характера. Микробные взаимоотношения при смешанных (или микст-) инфекциях вариабельны:
Если микроорганизмы активизируют или отягощают течение болезни, их определяют как активаторы, или синергисты (например, вирусы гриппа и стрептококки группы Б);
Если микроорганизмы взаимно подавляют патогенное действие, их обозначают как антагонисты (например, кишечная палочка подавляет активность патогенных сальмонелл, шигелл, стрептококков и стафилококков);
Индифферентные микроорганизмы не влияют на активность других возбудителей.
Манифестные инфекции могут протекать типично, атипично или хронически.
Типичная инфекция . После попадания в организм инфекционный агент размножается и вызывает развитие характерных патологических процессов и клинических проявлений.
Атипичная инфекция . Возбудитель размножается в организме, но не вызывает развития типичных патологических процессов, а клинические проявления носят невыраженный, стёртый характер. Атипичность инфекционного процесса может быть вызвана пониженной вирулентностью возбудителя, активным противодействием защитных факторов его патогенным потенциям, влиянием проводимой антимикробной терапии и совокупностью указанных факторов.
Хроническая инфекция обычно развивается после инфицирования микроорганизмами, способными к длительному персистированию. В ряде случаев под влиянием антимикробной терапии либо под действием защитных механизмов бактерии преобразуются в L-формы. При этом они лишаются клеточной стенки, а вместе с ней и структур, распознаваемых AT и служащих мишенями для многих антибиотиков. Другие бактерии способны длительно циркулировать в организме, «уходя» от действия указанных факторов за счёт антигенной мимикрии или изменения антигенной структуры. Подобные ситуации известны также как персистирующие инфекции [от лат. persisto, persistens, выживать, выдерживать]. По окончании химиотерапии L-формы могут возвращаться к исходному (вирулентному) типу, а виды, способные к длительному персистированию, начинают размножаться, что и вызывает вторичное обострение, рецидив болезни.
Медленные инфекции . Само название отражает медленную (в течение многих месяцев и лет) динамику инфекционного заболевания. Возбудитель (обычно вирус) проникает в организм и латентно присутствует в клетках. Под влиянием различных факторов инфекционный агент начинает размножаться (при этом скорость репродукции остаётся невысокой), заболевание принимает клинически выраженную форму, тяжесть которой постепенно усиливается, приводя к гибели пациента.
В подавляющем большинстве случаев патогенные микроорганизмы попадают в неблагоприятные условия различных областей организма, где погибают либо подвергаются действию защитных механизмов или элиминируются чисто механически. В некоторых случаях возбудитель задерживается в организме, но подвергается такому «сдерживающему» давлению, что не проявляет патогенных свойств и не вызывает развития клинических проявлений (абортивные, скрытые, «дремлющие» инфекции ).
Абортивная инфекция [от лат. aborto, не вынашивать, в данном контексте - не реализовывать патогенный потенциал] - одна из наиболее распространённых форм бессимптомных поражений. Такие процессы могут возникать при видовой или внутривидовой, естественной либо искусственной невосприимчивости (поэтому человек не болеет многими болезнями животных). Механизмы невосприимчивости эффективно блокируют жизнедеятельность микроорганизмов, возбудитель не размножается в организме, инфекционный цикл возбудителя прерывается, он погибает и удаляется из макроорганизма.
Латентная, или скрытая , инфекция [от лат. latentis, спрятанный] - ограниченный процесс с длительной и циклической циркуляцией возбудителя, аналогичной наблюдаемой при явных формах инфекционного процесса. Возбудитель размножается в организме; вызывает развитие защитных реакций, выводится из организма, но никаких клинических проявлений не наблюдают. Подобные состояния также известны как инаппарантные инфекции (от англ. inapparent, неявный, неразличимый). Так, нередко в латентной форме протекают вирусные гепатиты, полиомиелит, герпетические инфекции и т.д. Лица с латентными инфекционными поражениями представляют эпидемическую опасность для окружающих.
Дремлющие инфекции могут быть разновидностью латентных инфекций или состояниями после перенесённого клинически выраженного заболевания. Обычно при этом устанавливается клинически не проявляемый баланс между патогенными потенциями возбудителя и защитными системами организма. Однако под влиянием различных факторов, понижающих резистентность (стрессы, переохлаждения, нарушения питания и т.д.), микроорганизмы приобретают возможность оказывать патогенное действие. Таким образом, лица, переносящие дремлющие инфекции, - резервуар и источник патогена.
Микробоносительство . Как следствие латентной инфекции или после перенесённого заболевания возбудитель «задерживается» в организме, но подвергается такому «сдерживающему давлению», что не проявляет патогенных свойств и не вызывает развития клинических проявлений. Такое состояние называется микробоносительство. Подобные субъекты выделяют патогенные микроорганизмы в окружающую среду и представляют большую опасность для окружающих лиц. Выделяют острое (до 3 мес), затяжное (до 6 мес) и хроническое (более б мес) микробоносительство. Носители играют большую роль в эпидемиологии многих кишечных инфекций - брюшного тифа, дизентерии, холеры и др.
Инфекция – это совокупность биологических реакций, которыми макроорганизм отвечает на внедрение возбудителя.
Диапазон проявлений инфекций может быть различным. Крайними формами проявления инфекций являются:
1) бактерионосительство, персистенция, живая вакцинация;
2) инфекционная болезнь; имеются клинические проявления инфекции, эти реакции могут привести к летальному исходу.
Инфекционный процесс – ответная реакция коллектива популяции на внедрение и циркуляцию в ней микробных агентов.
Инфекционные болезни имеют ряд характерных особенностей, отличающих их от других болезней:
1) инфекционные болезни имеют своего возбудителя – микроорганизм;
2) инфекционные болезни контагиозны, т. е. способны передаваться от больного к здоровому;
3) инфекционные болезни оставляют после себя более или менее выраженную невосприимчивость или повышенную чувствительность к данному заболеванию;
4) для инфекционных болезней характерен ряд общих признаков: лихорадка, симптомы общей интоксикации, вялость, адинамия;
5) инфекционные болезни имеют четко выраженную стадийность, этапность.
Для возникновения инфекционного заболевания необходимо сочетание следующих факторов:
1) наличия микробного агента;
2) восприимчивости макроорганизма;
3) наличия среды, в которой происходит это взаимодействие.
Микробный агент – это патогенные и условно-патогенные микроорганизмы.
Существенное значение для возникновения инфекционного заболевания имеет инфицирующая доза возбудителя – минимальное количество микробных клеток, способных вызвать инфекционный процесс. Инфицирующие дозы зависят от видовой принадлежности возбудителя, его вирулентности и состояния неспецифической и иммунной защиты.
Ткани, лишенные физиологической защиты против конкретного вида микроорганизма, служат местом его проникновения в макроорганизм, или входными воротами инфекции. Входные ворота определяют локализацию возбудителя в организме, патогенетические и клинические особенности заболевания.
Внешняя среда может оказывать влияние как на макроорганизм, так и на микробов-возбудителей. Это природно-климатические, социально-экономические, культурно-бытовые условия.
Для ряда инфекций характерны эпидемии и пандемии.
Эпидемия – это широкое распространение инфекции в популяции с охватом больших территорий, характеризующееся массовостью заболеваний.
Пандемия – распространение инфекции практически на всю территорию земного шара с очень высоким процентом случаев заболеваний.
Эндемичные заболевания (с природной очаговостью) – это заболевания, для которых отмечены территориальные ареалы с повышенной заболеваемостью данной инфекцией.
2. Формы инфекции и периоды инфекционных болезней
Классификация инфекций
1. По этиологии:
1) бактериальные;
2) вирусные;
3) протозойные;
4) микозы;
5) микст-инфекции.
2. По количеству возбудителей:
1) моноинфекции;
2) полиинфекции.
3. По тяжести течения:
1) легкие;
2) тяжелые;
3) средней тяжести.
4. По длительности:
1) острые;
2) подострые;
3) хронические;
4) латентные.
5. По путям передачи:
1) горизонтальные:
а) воздушно-капельный путь;
б) фекально-оральный;
в) контактный;
г) трансмиссивный;
д) половой;
2) вертикальные:
а) от матери к плоду (трансплацентарный);
б) от матери к новорожденному в родовом акте;
3) артифициальные (искусственные) – при инъекциях, обследованиях, операциях и т. д.
В зависимости от локализации возбудителя различают:
1) очаговую инфекцию, при которой микроорганизмы локализуются в местном очаге и не распространяются по всему организму;
2) генерализованную инфекцию, при которой возбудитель распространяется по организму лимфогенным и гематогенным путем. При этом развивается бактериемия или вирусемия. Наиболее тяжелая форма – сепсис.
Выделяют также:
1) экзогенные инфекции; возникают в результате заражения человека патогенными микроорганизмами, поступающими из окружающей среды с пищей, водой, воздухом, почвой, выделениями больного человека, реконвалесцента и микробоносителя;
2) эндогенные инфекции; вызываются представителями нормальной микрофлоры – условно-патогенными микроорганизмами самого индивидуума.
Разновидность эндогенных инфекций – аутоинфекции, они возникают в результате самозаражения путем переноса возбудителя из одного биотопа в другой.
Выделяют следующие периоды инфекционных болезней:
1) инкубационный; от момента проникновения возбудителя в организм до появления первых признаков заболевания. Продолжительность – от нескольких часов до нескольких недель. Больной не заразен;
2) продромальный; характеризуется появлением первых неясных общих симптомов. Возбудитель интенсивно размножается, колонизирует ткань, начинает продуцировать ферменты и токсины. Продолжительность – от нескольких часов до нескольких дней;
3) разгар болезни; характеризуется появлением специфических симптомов. Возбудитель продолжает интенсивно размножаться, накапливаться, выделяет в кровь токсины и ферменты. Происходит выделение возбудителя из организма, поэтому больной представляет опасность для окружающих. В начале данного периода в крови обнаруживаются специфические антитела;
4) исход. Могут быть разные варианты:
а) летальный исход;
б) выздоровление (клиническое и микробиологическое). Клиническое выздоровление: симптомы заболевания угасли, но возбудитель еще находится в организме. Этот вариант опасен формированием носительства и рецидивом заболевания. Микробиологическое – полное выздоровление; в) хроническое носительство.
Реинфекцией называют заболевание, возникающее после перенесенной инфекции в случае повторного заражения тем же возбудителем.
Суперинфекция возникает, когда на фоне течения одного инфекционного заболевания происходит заражение еще одним возбудителем.
3. Возбудители инфекций и их свойства
Среди бактерий по способности вызывать заболевание выделяют:
1) патогенные;
2) условно-патогенные;
Патогенные виды потенциально способны вызывать инфекционное заболевание.
Патогенность – это способность микроорганизмов, попадая в организм, вызывать в его тканях и органах патологические изменения. Это качественный видовой признак, детерминированный генами патогенности – вирулонами. Они могут локализоваться в хромосомах, плазмидах, транспозонах.
Условно-патогенные бактерии могут вызывать инфекционное заболевание при снижении защитных сил организма.
Сапрофитные бактерии никогда не вызывают заболевания, так как они не способны размножаться в тканях макроорганизма.
Реализация патогенности идет через вирулентность – это способность микроорганизма проникать в макроорганизм, размножаться в нем и подавлять его защитные свойства.
Это штаммовый признак, он поддается количественной характеристике. Вирулентность – фенотипическое проявление патогенности.
Количественными характеристиками вирулентности являются:
1) DLM (минимальная летальная доза) – это количество бактерий, при введении которых соответствующим путем в организм лабораторных животных получают 95–98 % гибели животных в эксперименте;
2) LD 50 – это количество бактерий, вызывающее гибель 50 % животных в эксперименте;
3) DCL (смертельная доза) вызывает 100 %-ную гибель животных в эксперименте.
К факторам вирулентности относят:
1) адгезию – способность бактерий прикрепляться к эпителиальным клеткам. Факторами адгезии являются реснички адгезии, адгезивные белки, липополисахариды у грамотрицательных бактерий, тейхоевые кислоты у грамположительных бактерий, у вирусов – специфические структуры белковой или полисахаридной природы;
2) колонизацию – способность размножаться на поверхности клеток, что ведет к накоплению бактерий;
3) пенетрацию – способность проникать в клетки;
4) инвазию – способность проникать в подлежащие ткани. Эта способность связана с продукцией таких ферментов, как гиалуронидаза и нейраминидаза;
5) агрессию – способность противостоять факторам неспецифической и иммунной защиты организма.
К факторам агрессии относят:
1) вещества разной природы, входящие в состав поверхностных структур клетки: капсулы, поверхностные белки и т. д. Многие из них подавляют миграцию лейкоцитов, препятствуя фагоцитозу;
2) ферменты – протеазы, коагулазу, фибринолизин, лецитиназу;
3) токсины, которые делят на экзо– и эндотоксины.
Экзотоксины – высокоядовитые белки. Они термолабильны, являются сильными антигенами, на которые в организме вырабатываются антитела, вступающие в реакции токсинонейтрализации. Этот признак кодируется плазмидами или генами профагов.
Эндотоксины – сложные комплексы липополисахаридной природы. Они термостабильны, являются слабыми антигенами, обладают общетоксическим действием. Кодируются хромосомными генами.